2nd June 2021 | Author: Dr Louise Hughes
バイオロジカルSEMは、表面構造のみを観察する比較的ニッチなアプリケーションから、TEMに近い解像度で組織や細胞の内部構造を3次元的に観察できるようになり、過去10年間で独自の地位を確立しました。生物学者が特に興味を持つ技術がいくつかあります。
SEMでのSTEM分析
バイオロジカル電子顕微鏡におけるコントラストは、現在の課題です。 この問題に対処するには、コントラストを向上させるためのサンプル準備の最適化、組成情報の利用(下記のマルチカラーSEMを参照)、顕微鏡の動作条件の最適化など、多くの方法があります。 TEMの加速電圧を下げると、試料のコントラストが大幅に向上しますが、SEMのような低い加速電圧(<1~30kV)には到達できません。 SEMに搭載された専用のSTEMホルダーとSTEM検出器は、切片試料を透過した電子の検出を再現し、その結果、コントラストの低い試料の撮像、試料の汚染の低減、試料の帯電の低減、さらには試料の損傷の低減が可能となります。 SEMにおけるSTEMは、TEMで達成できるような解像度を持たないというトレードオフがありますが、わずかに低い解像度のアプリケーションのためにSEMの機能を拡張することにもなります。
ブロックフェイス・イメージング
また樹脂に埋め込まれた試料の平面からも、試料の超微細な情報を得ることができます。 樹脂ブロックの切断面や研磨面から後方散乱電子像を得ることができ、試料の超微細構造情報を得ることができます。 SEMのTEMやSTEMと比較して、ブロックフェイスイメージングの利点は、グリッドバーなどの支持材に邪魔されることなく、広い面積をイメージングできることです。 非常に低い加速電圧と長いビーム滞留時間により、高解像度の画像を得ることができます。 ビーム感度やチャージアップの問題から、この種のサンプルで最高のイメージング結果を得るためには、イメージング条件が非常に重要になります。
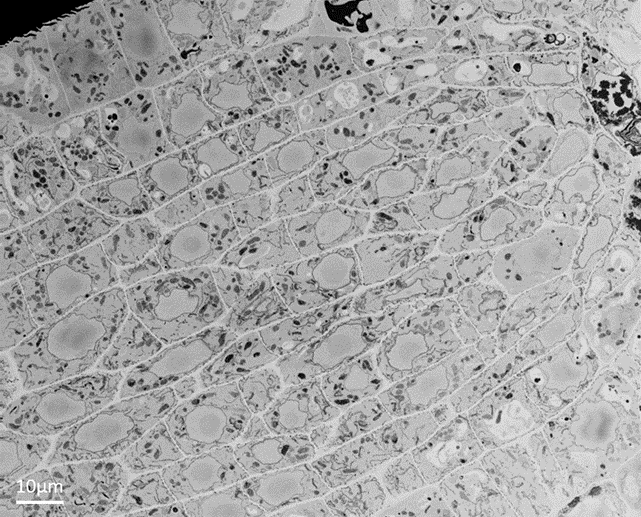
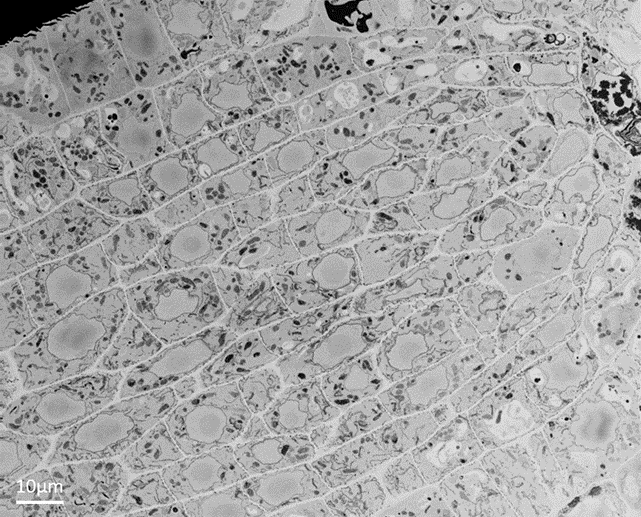
図 1. 後方散乱電子で撮影されたシロイヌナズナの根の先端部のブロックフェイス画像で、細胞の超微細構造がわかります。
ボリュームSEM
ボリューム顕微鏡は、TEM(シリアルセクションTEM、電子線トモグラフィー)でも行うことができますが、細胞やオルガネラの一部など、比較的小さな体積の試料に限られます。 ボリュームSEMは、細胞全体、組織の広い範囲、あるいは生物全体の超微細構造のデータを必要とするボリュームに対して、さまざまな技術を提供します。 ボリュームSEMの手法については、以前のブログ記事で紹介しています。 最も一般的に使用されている3つの手法は、試料をスライスし、スライス部分または残りの試料ブロックのいずれかの画像を撮影するものです(シリアルブロックフェイスイメージング)。
- 集束イオンビーム走査電子顕微鏡(FIBSEM)は、デュアルビーム顕微鏡を使用しています。電子ビームでサンプルの表面を撮影します。一方イオンビームは、2つの電子線像を取得する間に、試料表面の薄い層を削ります。
- シリアルブロックフェイス走査型電子顕微鏡(SBFSEM)では、撮影の合間にダイヤモンドナイフを使って試料の表面層を取ります。
- アレイ・トモグラフィー(またはシリアルセクションSEM)は、顕微鏡の外で一連のスライスまたは断片を作成し、それらを基板上に保存し、各スライスを順次イメージングするものです。
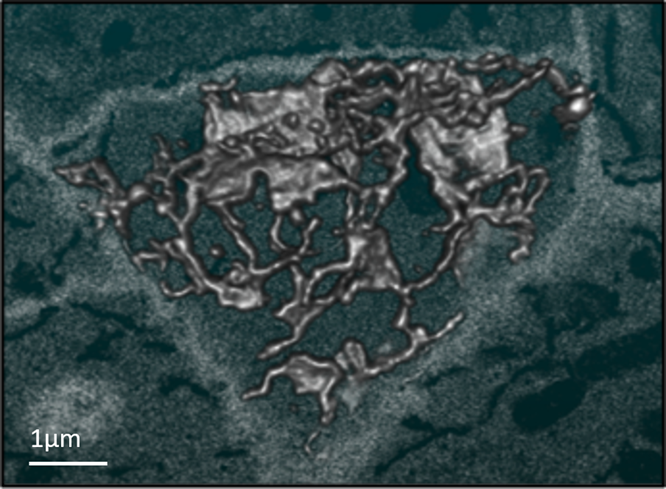
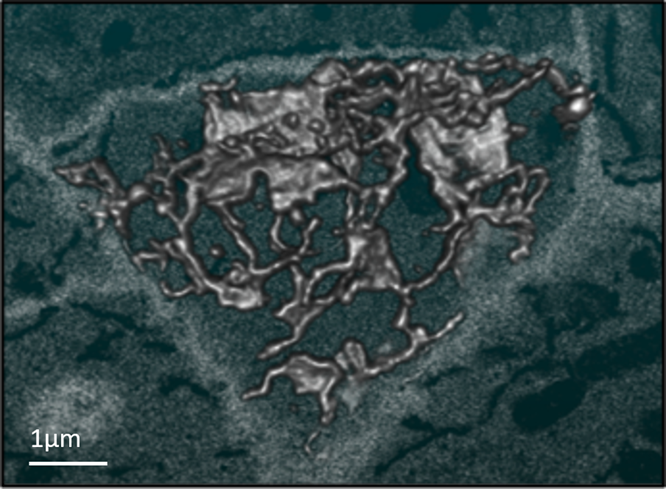
図 2. 根の細胞の端にある小胞体を3次元的に再構成したSBFSEMデータ。図1に示したのと同じ標本から撮影したデータ。
それぞれのボリュームSEM技術は、従来の2D電子画像では解析が非常に困難であった複雑な3D超微細構造の正確な解釈とモデル化を容易にするデータを提供します。
クライオSEM
Cryo-SEMでは、特別に冷却されたステージとサンプル搬送装置を使用して、完全に水和して凍結したサンプルを、できるだけ自然な状態に近い状態で撮影します。 すべてのバイオロジカル電子顕微鏡の大きな課題は、高真空とダメージを与える電子ビームという過酷な電子顕微鏡環境にさらされた試料を保存するために必要な大がかりな試料調製です。 試料を急速に凍結して氷晶の形成を避け、水分をガラス状にすることで、可能な限り迅速な保存を実現し、試料中のアーティファクトを最小限に抑えることができます。 Cryo-SEMは、光ー電子相関顕微鏡法(CLEM)やFIBSEMなどの他の技術と組み合わせて使用することで、凍結したサンプルを3Dでイメージングしたり、高解像度TEM用の薄い凍結サンプルのスライスを作成したりすることができます。
マルチカラーSEM
電子信号による構造情報を画像化し、生体試料の組成情報と組み合わせることが可能です。 この組成データは、エネルギー分散型X線分析(EDS)、電子エネルギー損失分光法(EELS)、カソードルミネッセンスを用いて得ることができ、色を適用することで電子データに応用することができます。 これらの技術は、サンプルに含まれる元素の同定、その分布のマッピング、相対的な量の測定に使用できます。生物学研究のためのEDSの詳細については、アプリケーションページをご覧ください。

図 3. 形状を示す二次電子(SE)画像、密度の違いを示す後方散乱電子(BSE)画像、および骨インプラント内の元素分布を示すX線信号の違いを示したもの(サンプル提供:Zhidao Xia, Swansea University)。
生物学者が利用可能な様々なSEM技術は、SEMが生物試料イメージング施設の重要なツールであることを意味します。 先端のバイオロジカルSEMについてより詳しく知りたい方は、次回のウェビナーにご登録下さい。 当日は、これらのトピックに加えて、撮影条件やサンプル作成技術を最適化することで、顕微鏡を最大限に活用する方法についてもお話しする予定です。